Et quelles sont les menaces?
Yves Dandonneau
1 - Le carbone, puits et source d’énergie
3 - L’absorption du rayonnement infra rouge par le gaz carbonique et les autres gaz à effet de serre
4 - Concentration et pression partielle de gaz carbonique et quelques raccourcis de calcul
5 - Le cycle naturel du carbone : puits et sources de gaz carbonique
6 - La perturbation anthropique et le cycle du carbone
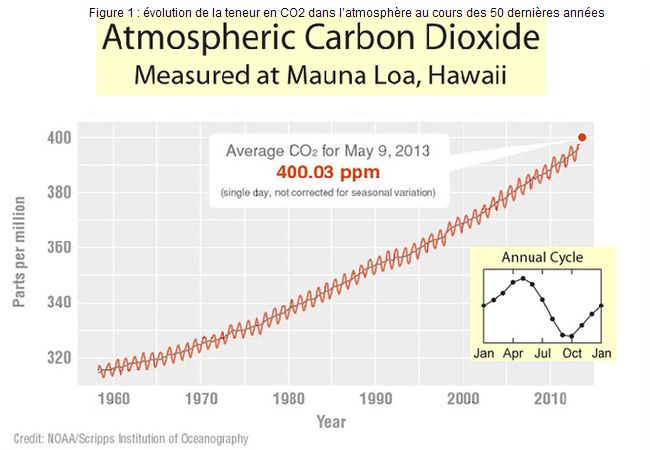
Le carbone est un élément très abondant dans les roches terrestres, l’eau et l’atmosphère. Il a tendance à se combiner à l’oxygène pour donner du gaz carbonique (CO2) en dégageant de la chaleur, et cette réaction fournit l’essentiel de l’énergie utilisée par l’homme. Le CO2 absorbe le rayonnement infra rouge et cette propriété contribue à déterminer la température à la surface de la Terre, là où nous vivons. Du fait des activités humaines, la teneur en CO2 de l’atmosphère augmente donc (figure 1), et cette augmentation entraîne un réchauffement du climat.
Soluble dans l’eau, intervenant dans les réactions géochimiques ainsi que dans celles de la vie, le carbone suit des cycles complexes qu’il faut connaître pour prévoir comment évoluera le climat en réponse à la perturbation anthropique.
1 - Le carbone, puits et source d’énergie
En brulant du carbone (c'est-à-dire en le combinant à l’oxygène), on obtient de l’énergie. L’état d’oxydation le plus abouti est le gaz carbonique. Entre le carbone et le gaz carbonique, il existe une multitude de formes plus ou moins oxydées, la plupart d’entre elles résultant de réactions du monde vivant.
Le tableau I donne la chaleur produite par quelques formes du carbone. On remarque que la combustion d’une mole de méthane (CH4) produit environ deux fois plus de chaleur que celle d’un atome de carbone graphite : la raison est que pour le méthane, l’oxydation du carbone s’accompagne de celle de 4 atomes d’hydrogène. Celle d’une mole d’éthanol (C2H5OH) en produit plus de trois fois plus : en plus de l’hydrogène qu’elle contient, elle comprend deux atomes de carbone. Si on décompose la combustion du carbone en
-
production de monoxyde de carbone (CO),
puis -
production de gaz carbonique, cette seconde combustion dégage à elle seule près des trois quarts de l’énergie produite par la combustion de carbone en gaz carbonique.
|
MégaJoule/kg |
kWh/kg |
kiloJoule/mole |
|
|
Graphite |
33 |
9 |
394 |
|
Méthane |
50 |
14 |
802 |
|
Ethanol |
29 |
8 |
1 330 |
|
Monoxyde de carbone |
10 |
3 |
283 |
Tableau I : Chaleur spécifique de combustion de quelques formes de carbone
Les réactions chimiques qui produisent du gaz carbonique dégagent de la chaleur.
Inversement, pour réduire du gaz carbonique, il faut fournir de l’énergie. Ainsi, l’oxygène étant abondant à la surface de la terre, la totalité du carbone devrait à terme se trouver sous forme de gaz carbonique. Ce n’est pas le cas, à cause de la photosynthèse opérée par les végétaux terrestres, les algues et les cyanobactéries, par laquelle le gaz carbonique est réduit en hydrates de carbone selon la réaction simplifiée suivante :
6 CO2 + 6 H2O ←→ C6H1206 + 6 O2 (1)
C’est l’énergie lumineuse, par l’intermédiaire de la chlorophylle, qui permet cette réaction. La respiration, la mort des cellules et leur décomposition, ramènent le carbone de sa forme réduite à la forme stable gaz carbonique. Toutefois, localement, dans certaines niches où l’oxygène manque, une petite fraction de ces hydrates de carbone reste préservée de l’oxydation : c’est ainsi que se sont lentement formés les gisements de charbon et de pétrole au cours des ères géologiques, gisements que l’activité humaine exploite à une vitesse folle, réinjectant dans l’atmosphère le gaz carbonique des ères géologiques passées.
2 - Les isotopes du carbone
Le carbone comporte six électrons et six protons, et, sous sa forme la plus abondante (98,89 %), six neutrons, ce qui lui confère une masse atomique de 12. Environ 1,1 % des atomes de carbone contiennent sept neutrons : c’est le carbone 13. Ces deux isotopes sont stables, au contraire du troisième isotope, le carbone 14, radioactif, de période 5 730 ans, formé dans la haute atmosphère par substitution d’un proton par un neutron dans un atome d’azote. Lors de sa décomposition par radioactivité, le noyau du carbone 14 émet un électron, revenant ainsi à l’état du noyau d’azote.
La plus ou moins grande abondance de ces isotopes n’a aucun effet sur le climat, mais témoigne de certains processus :
-
Les molécules de gaz carbonique qui ont un atome de carbone 13 sont plus lourdes et ont davantage d’inertie que celles, beaucoup plus nombreuses, qui ont l’isotope 12, et ont donc une probabilité moindre d’être captées par la réaction de photosynthèse. La matière vivante est donc de ce fait appauvrie en isotope 13 par rapport au milieu environnant, et cette particularité est préservée dans les gisements de charbon et de pétrole. De ce fait, lorsqu’on brûle du pétrole, les masses d’air contaminées par le gaz carbonique émis portent la signature de ce fractionnement isotopique ancien. Les mesures de concentration en 13CO2 dans l’atmosphère permettent de calibrer les modèles d’émission de gaz carbonique et de circulation atmosphérique.
-
Dans les années 60 ont eu lieu des expérimentations nucléaires dans l’atmosphère, qui ont émis de grandes quantités de carbone 14. Une part de ce carbone 14 a été oxydée en gaz carbonique 14CO2, qui s’est comporté comme 12CO2 ou 13CO2 et a pénétré les océans. La mesure de la concentration en carbone 14 en de nombreux points de l’océan, représentatifs de sa totalité, a permis d’estimer à 2,2 GT de carbone la part des émissions humaines absorbée chaque année par les océans.
3 - L’absorption du rayonnement infra rouge par le gaz carbonique et les autres gaz à effet de serre
Composées de deux atomes, les molécules d’azote et d’oxygène, qui composent la quasi-totalité de l’atmosphère, sont transparentes pour le rayonnement infra rouge, de longueur d’onde comprise entre 4 et 70 microns environ émis par la Terre. Mais l’atmosphère contient aussi, en quantité moindre, des gaz dont les molécules sont composées de trois atomes ou plus, qui absorbent ce rayonnement. Au premier rang d’entre eux, la vapeur d’eau, relativement abondante, mais en quantité variable. Elle correspond à un stade du cycle naturel de l’eau sur terre, et en première approche, on peut considérer que son rôle dans le transfert du rayonnement infra rouge n’est pas affecté par le changement climatique en cours. Il n’en va pas de même pour le gaz carbonique dont la concentration dans l’atmosphère augmente régulièrement du fait des activités humaines. Le spectre d’absorption du gaz carbonique présente des bandes dans lesquelles ce rayonnement est fortement absorbé, vers 4 et 15 microns notamment. Lorsqu’un photon infra rouge émis par la Terre est intercepté par une molécule de gaz carbonique, il est aussitôt réémis sous la forme d’un autre photon infra rouge, mais celui-ci, au lieu de s’échapper vers l’espace, a 50 % de chances d’être renvoyé vers la surface de la Terre qu’il contribue alors à chauffer. La chaleur additionnelle acquise par la surface de la Terre se propage dans l’atmosphère par conduction thermique et convection : c’est ce processus qui constitue l’effet de serre.
Le gaz carbonique n’est pas le seul gaz à effet de serre dont l’activité humaine fait croître la concentration dans l’atmosphère. Le plus puissant est le protoxyde d’azote N2O, appelé aussi «gaz hilarant» émis principalement par l’usage d’engrais azotés en agriculture, mais aussi par certains procédés industriels : à concentration égale, le protoxyde d’azote absorbe environ 300 fois plus d’énergie infra rouge que le gaz carbonique. Le méthane, CH4, en augmentation lui aussi du fait des pratiques agricoles (l’élevage et les rizières) est lui aussi un gaz à effet de serre beaucoup plus puissant que le gaz carbonique (environ 90 fois). Enfin, les lourdes molécules d'halocarbures, certains utilisés autrefois, mais maintenant interdits, comme gaz réfrigérants, ont un énorme pouvoir absorbant et leur durée de vie dans l’atmosphère dépasse le millier d’années. Heureusement, ils sont en concentration très faible. L’effet de la présence de tous ces gaz dans l’atmosphère sur le climat dépend bien sûr de leurs concentrations respectives, mais aussi de leur durée de vie : une même quantité de gaz introduite dans l’atmosphère n’aura évidemment pas le même effet sur le climat selon qu’elle y persiste 100 ans ou 1 000 ans. Afin de pouvoir évaluer cet effet, on a donc introduit la notion d’équivalent carbone (tableau II). 1 kg de méthane, 90 fois plus puissant que le gaz carbonique en termes d’effet de serre, mais dont le temps de résidence dans l’atmosphère est très inférieur, aura le même effet que 25 kg de gaz carbonique où que 6,8 kg de carbone (1 kg de gaz carbonique contient 0,27 kg de carbone) ; on dit alors que 1 kg de méthane vaut 6,8 équivalents carbone.
|
Temps de résidence approximatif dans l’atmosphère |
Équivalent carbone |
|
|
Gaz carbonique |
100 ans |
0,27 |
|
Méthane |
12 ans |
6,8 |
|
Protoxyde d’azote |
120 ans |
81,3 |
|
Halocarbures |
Jusqu'à 50 000 ans pour certains |
34 à 6 220 |
Tableau II : Propriétés des principaux gaz à effet de serre d’origine humaine
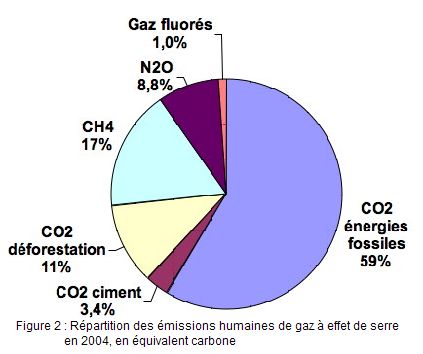
Bien que le gaz carbonique soit beaucoup moins efficace en termes d'effet de serre que d’autres gaz, il est beaucoup plus abondant, et est responsable des trois quarts de l’effet de serre (voir figure 2).
4 - Concentration et pression partielle de gaz carbonique et quelques raccourcis de calcul
Dans l’atmosphère, la concentration en gaz carbonique s’exprime simplement en moles (ou parties) par million (ppm). Rapportée à tous les gaz de l’atmosphère cette concentration peut varier selon les ajouts ou la condensation de vapeur d’eau dont le temps de résidence dans l’atmosphère est assez bref. Aussi exprime-t-on cette concentration par rapport à de l’air sec. C’est ainsi qu’elle est représentée sur la figure 1.
Une autre notion est importante car c’est elle qui détermine les échanges de gaz entre l’atmosphère et les océans : la pression partielle (pCO2). Dans l’atmosphère, si la pression atmosphérique est «normale» (760 mm de mercure, ou 1,01325 bar) et s’il n’y a pas de vapeur d’eau, la pression partielle s’exprime en microatmosphère (µatm) par le même nombre que la concentration en ppm. Dans les conditions usuelles, la pression partielle de gaz carbonique est égale au produit de la pression atmosphérique par la concentration de ce gaz dans l’atmosphère, vapeur d’eau comprise.
Dans l’océan, la pression partielle de gaz carbonique est égale à celle mesurée dans un volume d’air équilibré avec l’eau de mer. Cette mesure n’a d’intérêt qu’à l’interface océan-atmosphère à travers laquelle se produisent les échanges gazeux, et où l’atmosphère est à la même température que la surface de l’océan et saturée en vapeur d’eau. Le flux de gaz carbonique se fait du milieu dans lequel la pression partielle est la plus élevée vers celui où elle est la plus faible, et est proportionnel à la différence de pression partielle, et à un coefficient d’échange qui dépend de la vitesse du vent.
L’océan et l’atmosphère se côtoyant depuis «belle lurette», ces deux milieux se sont équilibrés, avec, toutefois, des écarts de pression partielle qui peuvent localement et saisonnièrement excéder 100 µatm selon la circulation océanique et les variations de température (cet équilibre, avant l’ère industrielle, se situait aux environs de 280 µatm). La pression partielle de gaz carbonique dans l’eau de mer varie en effet avec la solubilité de ce gaz, laquelle est surtout fonction de la température. Elle varie aussi selon l’état du H2O + CO2 ←→ H+ = HCO3- ←→ 2 H+ + CO32- (2)
Un retrait de gaz carbonique (par photosynthèse par exemple, voir réaction (1) où un retrait de carbonate (CO32-, par fabrication de calcaire) déplaceront cet équilibre dans le sens d’une atténuation de la perturbation. Une écriture simplifiée de l’équilibre (2) met en évidence le comportement dominant des carbonates et permet de comprendre les variations de la pression partielle de gaz carbonique face aux perturbations ;
2 HCO3- ←→ H2O + CO32- + CO2 (3)
Ainsi, un déséquilibre dû à un apport de gaz carbonique dans l’eau, c'est-à-dire un ajout à la partie de droite de l’équilibre, actionnera cette réaction vers la gauche : le déséquilibre sera corrigé par la fabrication d’ions bicarbonate HCO3-, accompagnée d’une acidification de l’eau. Un retrait de carbonate CO32-, c'est-à-dire un retrait à la partie gauche, qui se produit lorsque des organismes fabriquent du calcaire entraînera par compensation une diminution des ions bicarbonate, et une augmentation du gaz carbonique dissous et par conséquent, de sa pression partielle. On appelle «carbone inorganique total» la somme gaz carbonique + carbonate + bicarbonate.
Le calcul de ces équilibres est assez complexe, mais il existe des relations empiriques simples qui répondent aux questions qu’on se pose le plus fréquemment.
La première permet de calculer la réponse de la pression partielle de gaz carbonique dans l’eau à une variation de température Δt :
pCO2 (t + Δt) = pCO2 (t) (1+ 0,023 Δt) (4)
Dit plus simplement, la pression partielle de gaz carbonique augmente de 2,3 % par degré.
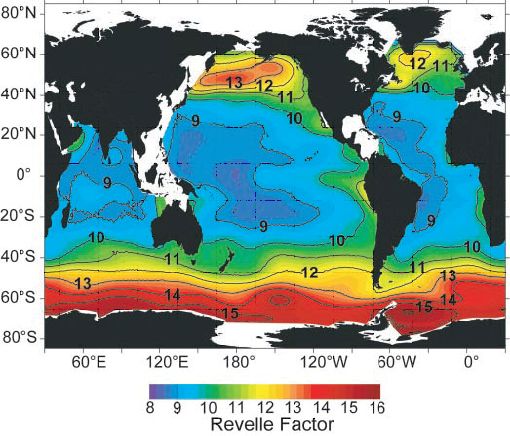
La seconde définit le «facteur de Revelle» comme le rapport de la variation relative de la pression partielle de gaz carbonique à la variation de la concentration en gaz carbonique + carbonates (TCO2) :
F = (ΔpCO2 / pCO2) (ΔTCO2 / TCO2)-1 (5)
Roger Revelle a cartographié ce rapport qui varie de manière très cohérente, dans l’océan (voir figure 3). On voit que la pression partielle de gaz carbonique se comporte comme un amplificateur des variations du contenu en carbone inorganique total de l’eau de mer (entre 1,8 et 2,5 mM/kg), variations qu’elle multiplie par 8 à 16 selon les zones de l’océan.
Figure 3 : variation du facteur de Revelle dans l’océan mondial
5 - Le cycle naturel du carbone : puits et sources de gaz carbonique
Les principaux flux de gaz carbonique entre l’atmosphère d’une part, et les océans et les terres émergées d’autre part, résultent de processus physiques (dissolution, transport et diffusion) et chimiques (transformations, équilibre avec les carbonates), ainsi que de l’activité biologique (photosynthèse, respiration). Le cycle dit « naturel » est celui, supposé stable, qui régnait avant l’ère industrielle, et mettait en jeu des sources de gaz carbonique égales aux puits.
-
Processus physiques et chimiques
Aux échelles de temps qui nous préoccupent, les processus physiques et chimiques d’échange de carbone entre les terres émergées d’une part, et l’atmosphère et les océans d’autre part, sont très faibles (voir figure 4) : il s’agit essentiellement d’altération des roches (0,2 Gt/an), et d’apport de gaz carbonique dissous dans l’eau de pluie (0,2 Gt/an), ces deux termes étant rejoints par 0,4 Gt/an de gaz carbonique issu de la décomposition des litières végétales, le tout étant entrainé vers l’océan par les fleuves.
Il n’en va pas de même entre l’atmosphère et l’océan dans lequel la dissolution du gaz carbonique, et son évasion sont à l’origine de flux importants (environ 70 Gt/an dans chaque sens). Pour l’essentiel, le flux d’évasion vers l’atmosphère est dû à des remontées d’eaux froides en surface, ce qui se produit surtout dans les zones d’upwelling tropicales ; ces eaux profondes qui sont riches en carbone inorganique total ont une pression partielle de gaz carbonique qui peut être bien plus élevée que celle de l’atmosphère, et cette différence est amplifiée par le réchauffement qu’elles subissent à ces basses latitudes où le rayonnement solaire est intense. L’absorption de gaz carbonique par l’océan s’effectue surtout aux hautes latitudes, lorsque les eaux qui dérivent vers les pôles, transportées par le Gulf Stream dans l’Atlantique nord ou par ses équivalents des autres bassins océaniques, se refroidit et voit donc sa pression partielle de gaz carbonique baisser et devenir inférieure à celle de l’atmosphère.
D’autre part, les mouvements au sein de l’océan sont à l’origine de flux de carbone inorganique total du même ordre de grandeur (90 Gt/an de l’océan superficiel vers l’océan profond, 100 Gt/an dans le sens inverse). Ces flux sont dus au mélange turbulent entre l’océan superficiel peu concentré en carbone inorganique total et l’océan profond plus concentré, et aussi à des transports massifs, vers le bas dans les hautes latitudes où se forment les eaux froides profondes, et vers le haut aux basses latitudes.
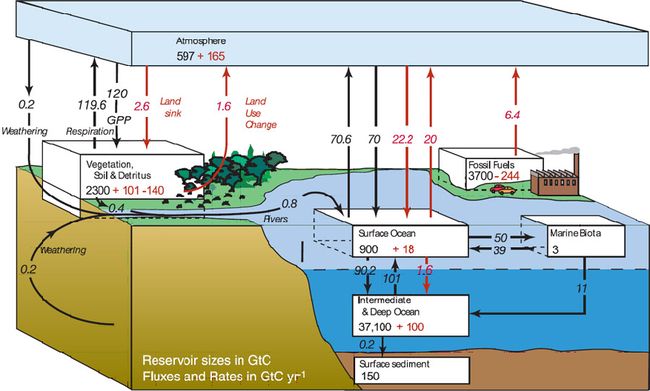
Figure 4 : Cycle global du carbone.
Les principaux flux annuels de l’époque pré-industrielle sont indiqués par les flèches noires, en GtC an–1, et les flux ‘anthropogéniques’ par les rouges. Les contenus en carbone des différents compartiments sont indiqués en GtC dans les rectangles blancs, en noir pour les stocks naturels, en rouge pour les changements intervenus depuis le début de l’ère industrielle (établi pour les années 90, 4ème rapport du GIEC).
-
Processus biologiques
Ces processus occasionnent des flux de gaz carbonique importants, que ce soit sur les terres émergées ou dans les océans, et leur bilan est à peu près nul, les flux de photosynthèse étant équilibrés par ceux de respiration et de dégradation de la matière organique : environ 120 Gt/an pour la vie terrestre (à l’origine des variations saisonnières dans l’atmosphère visibles sur la figure 1), et 50 Gt/an pour la vie océanique. La différence importante entre ces deux domaines est que sur les terres émergées, la matière organique qui résulte de la photosynthèse reste piégée dans les premières dizaines de cm du sol et au contact de l’atmosphère, tandis que dans l’océan, une partie des débris issus de la matière vivante sédimente vers l’océan profond et s’y décompose en libérant du gaz carbonique. C’est ce processus de sédimentation de la matière vivante qui est à l’origine de la différence entre un océan de surface pauvre en carbone inorganique total et un océan profond riche.
A noter dans l’océan un processus très lent et dont les résultats ne sont sensibles qu’aux échelles de temps géologiques : la biocalcification. Il s’agit de fabrication de pièces calcaires (CO32-, carbonate de calcium), coquilles de mollusques chez les Ptéropodes, ou coccolithes chez les algues microscopiques dites coccolithophoridés. Ces pièces calcaires sédimentent à travers la colonne d’eau, et celles qui parviennent à la surface du sédiment sans être totalement dissoutes retirent ainsi, peu à peu, du carbone au système océan – atmosphère – terres émergées. Paradoxalement, la biocalcification fait augmenter la pression partielle de gaz carbonique : on voit en effet qu’un retrait de carbonate de l’eau de mer actionne l’équilibre chimique (3) vers la droite, dégageant ainsi du gaz carbonique.
6 - La perturbation anthropique et le cycle du carbone
Depuis le début de l’ère industrielle, soit depuis 1860 environ, l’activité humaine utilise du carbone, sous forme de charbon, de pétrole ou de gaz, pour ses besoins en énergie. On a ainsi transformé en gaz carbonique, c'est-à-dire «brûlé» 244 Gt de carbone (voir figure 4), à raison de 6,4 GtC/an dans les années 90. Ce chiffre est maintenant largement dépassé : en 2012, ces émissions ont atteint 9,7 Gt, auxquelles s’ajoutent 0,4 Gt dues à la production de gaz carbonique lors de la calcination du calcaire dans la fabrication du ciment. S’y ajoutent également 1,6 Gt/an provenant d’un changement d’affectation des sols : lorsqu’une forêt est défrichée pour être transformée en champs, la biomasse constitutive de la forêt est brûlée et l’humus du sol est rapidement oxydé. Tous ces rejets de gaz carbonique dans l’atmosphère y font augmenter l’effet de serre naturel sont à l’origine du réchauffement global du climat. Cependant, une partie de ce gaz carbonique anthropique ne perdure pas dans l’atmosphère et est au contraire absorbée, selon deux processus principaux :
D’une part, une atmosphère riche en gaz carbonique stimule la photosynthèse et est favorable à la croissance des végétaux terrestre. Ainsi, la biomasse des végétaux sur les terres émergées tend à augmenter, au taux estimé de 2,6 GtC/an.
D’autre part, l’injection permanente de gaz carbonique dans l’atmosphère fait que la pression partielle de ce gaz est maintenue à une valeur supérieure à sa valeur moyenne dans l’océan, ce qui entraîne un flux additionnel de 2,2 GtC/an de l’atmosphère vers l’océan.
Les émissions anthropiques excèdent donc largement les capacités d’absorption (2,6 + 2,2 = 4,8 GtC/an) des systèmes naturels, et la concentration en gaz carbonique de l’atmosphère ne cesse d’augmenter (figure 1).
L’évolution de cette perturbation dépendra du rythme de nos émissions de gaz carbonique. Mais quel que soit ce rythme, la résorption de l’excès anthropique de gaz carbonique se fera surtout par l’océan et prendra beaucoup de temps : l’équilibre entre l’océan de surface (les 50 à 150 premiers mètres) et l’atmosphère s’établit assez rapidement, en six mois environ, puis est remis en question au fur à mesure que cet océan superficiel se mélange avec un océan profond dont le contenu en carbone inorganique total résulte d’un équilibre antérieur, préindustriel même en ce qui concerne l’océan très profond. On estime que si on stoppait totalement les émissions, il faudrait 30 ans pour en résorber la moitié, et que 50 ans plus tard, il en resterait encore 20 %.
7 - Questions et menaces
Un arrêt brutal des émissions de gaz carbonique n’est évidemment pas envisageable, et la concentration de ce gaz dans l’atmosphère continuera de croître. Les puits de carbone risquent alors de perdre en efficacité.
L’entrée de gaz carbonique, un gaz acide, dans l’océan y augmente l’acidité et y réduit donc la solubilité de ce gaz. Cet effet apparaît dans les variations du facteur de Revelle (figure 3) qui est plus élevé aux hautes latitudes qu’aux basses. La raison en est que le gaz carbonique est plus soluble dans les eaux froides des latitudes élevées qui en contiennent donc davantage et sont (on constate déjà une acidification des océans) plus acides. Dans ces eaux, l’ajout d’une même quantité de gaz carbonique y entraînera une augmentation plus grande de la pression partielle de gaz carbonique. Au final, un océan qui a absorbé tout ou partie du gaz carbonique anthropique sera plus acide et aura une pression partielle de gaz carbonique plus élevée : ce sera à l’atmosphère de s’y ajuster.
Un climat plus chaud peut s’avérer néfaste pour la végétation terrestre qui pourrait en souffrir. La capacité des écosystèmes terrestres à absorber une partie du gaz carbonique anthropique devrait alors diminuer, voire même s’annuler.
Sous un climat plus chaud, la matière organique des sols sera oxydée plus rapidement, occasionnant un dégagement de gaz carbonique dans l’atmosphère. Ceci est spécialement préoccupant aux latitudes élevées où d’importantes quantités de carbone organique sont piégées dans les sols gelés (pergélisols) ou dans les tourbières, principalement sous forme de méthane.
Enfin, jusqu’à preuve du contraire, les écosystèmes marins n’ont pas été affectés par le réchauffement climatique et ne jouent donc aucun rôle dans l’absorption du gaz carbonique anthropique (figure 4). Sous l’influence du réchauffement global, l’écart de température (et donc de densité) entre l’océan superficiel et l’océan profond devrait s’accroître, freinant les échanges turbulents entre ces deux couches, ou les remontées d’eaux profondes. Or, ce sont ces mélanges ou ces remontées qui fournissent les sels nutritifs nécessaires à la croissance des algues. Si la photosynthèse par ces algues diminue, ce n’est pas 11 GtC/an que cet écosystème émettra vers l’océan profond (figure 4), mais une quantité moindre, ce qui y ralentira l’exportation du carbone anthropique. On pourrait aussi assister à des modifications de cet écosystème marin sous ces nouvelles conditions, sans qu’il soit possible d’en prévoir dès maintenant les conséquences en termes de puits de carbone.
Si les grands traits du cycle du carbone sont relativement bien connus, les flux indiqués sur la figure 4 sont des estimations et souffrent souvent d’une forte imprécision. Les éléments les mieux connus sont les stocks de carbone dans les milieux fluides : atmosphère et océan, au sein desquels les mélanges conduisent à une certaine homogénéité. Les émissions anthropiques de carbone sont elles aussi connues avec précision via les données sur la consommation de pétrole, de charbon et de gaz. Mais les flux entre les compartiments atmosphère, océans, et terres émergées sont très difficiles à estimer à cause de leur très forte variabilité dans l’espace et le temps. Mieux connaître ces flux et leurs variations est indispensable pour comprendre et prévoir l’évolution du système climatique. Ceci passe par des mesures sur le terrain bien plus nombreuses que ce qu’on a pu réaliser jusqu’à présent, et qui ne pourront être réalisées que dans le cadre d’une action internationale coordonnée.
Voir aussi :
FAQ :
Quel est le rôle du gaz carbonique sur l'évolution du climat?
Y a-t-il saturation de l'effet de serre?
Dossier Climat :